Entwicklung von Reaktionsmechanismen unter Parameteridentifikation von Subsystemen
- Ansprechperson:
Dr.-Ing. Nadia Sebbar
- Projektgruppe:
Prof. Dr.-Ing. D. Trimis
Entwicklung von Reaktionsmechanismen unter Parameteridentifikation von Subsystemen
Berechnungsmethoden
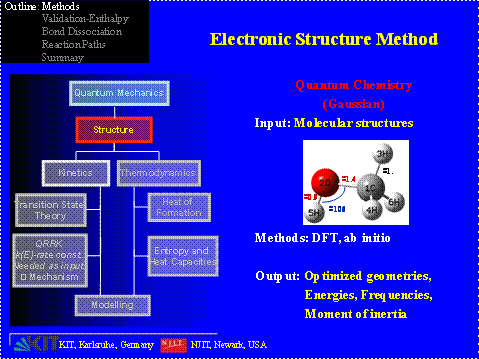
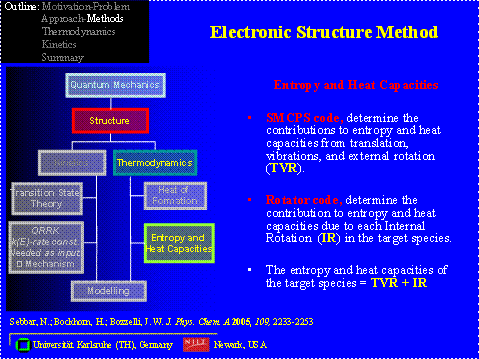
Alle Berechnungen werden mit dem Programm Gaussian 03 durchgeführt, das die Gesamtenergien, die Frequenzen und das Trägheitsmoment berechnet. Die Bestimmung der Entropien und Wärmekapazitäten werden mit Hilfe von zwei Codes berechnet: SMCPS und ROTATOR.
Hauptziele
Die Anwendung der rechnergestützten Quantenchemie (ab inito und DFT-Berechnungen) wird zur Abschätzung der thermochemischen Eigenschaften und der kinetischen Parameter kleiner und großer Spezies eingesetzt, darunter Biochemikalien, große aromatische Zwischenprodukte bei der Rußbildung, Kohlenstoff-Nanoröhren und viele andere Systeme.
Einführung
Aromatische und polyaromatische Verbindungen sind wichtige Bestandteile von Kraftstoffen. Sie werden auch bei Pyrolysereaktionen und in brennstoffreichen Bereichen von Flammen und anderen thermischen Systemen gebildet, wo sie als wichtige Vorläufer und Zwischenprodukte bei der Ruß- und PAK-Bildung gelten. Die Zersetzungsprodukte dieser Spezies in Verbrennungs- und Oxidationsreaktionen beinhalten die Einbindung von Sauerstoff durch Reaktionen mit sauerstoffhaltigen Radikalen und mit molekularem Sauerstoff, Spezies wie Hydroperoxide oder ungesättigte Oxy-Kohlenwasserstoffe bilden.
Im Rahmen dieser Arbeit wird eine umfangreiche Datenbank mit thermochemischen Eigenschaften ungesättigter (olefinischer, acetylenischer und aromatischer) sauerstoffhaltiger Kohlenwasserstoffspezies entwickelt: Es werden Bildungsenthalpie, Bindungsenergien, Standardentropie und Wärmekapazität in Abhängigkeit von der Temperatur berechnet. Diese Daten dienen den Modellierungsgemeinschaften im Bereich der Atmosphärenchemie, der Verbrennung, der industriellen Prozesse im Zusammenhang mit der Synthese und der Verwendung bei der Synthese von Hydroperoxiden, Peroxiden und radikalischen Peroxyspezies. Diese Parameter sind über einen weiten Temperaturbereich (200 bis über 5000 K) verfügbar, der auf alle oben genannten Bereiche angewendet werden kann.
Peroxide und Peroxyspezies sind vielleicht die wichtigsten Zwischenprodukte bei allen Verbrennungsvorgängen bei niedrigen und mittleren Temperaturen (1200 - 1300 K) und bei photochemischen Oxidationsprozessen von Kohlenwasserstoffen und Derivaten in der Atmosphäre. Beispiele für die Bedeutung dieser Peroxide und Peroxy-Zwischenprodukte sind: Kontrolle der Selbstzündung in Verbrennungsmotoren (Klopfen in Ottomotoren sowie Kraftstoffzündung in Dieselmotoren und in den neuen und künftigen HCCI-Motoren). Die chemische Reaktion der Peroxy-Radikale steuert auch das negative Temperaturverhalten von Kohlenwasserstoffen, bei dem ein Wettbewerb zwischen den komplexen Kettenverzweigungspfaden und Abbruchreaktionen stattfindet. Alkylhydroperoxid-Spezies spielen auch eine wichtige Rolle bei der Begrenzung der Rußbildung und beim Rußausbrand bei der Pyrolyse und Verbrennung von Kohlenwasserstoffen.
Für stabile Moleküle, intermediäre Radikale und Übergangszustandsstrukturen sauerstoffhaltiger Kohlenwasserstoffmoleküle, insbesondere ungesättigter und aromatischer Kohlenstoff-Sauerstoff-Systeme, wird eine sehr große Anzahl thermochemischer Parameter ermittelt.
Beispiel der Arbeit
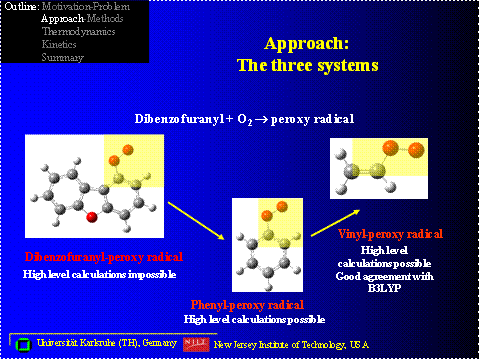
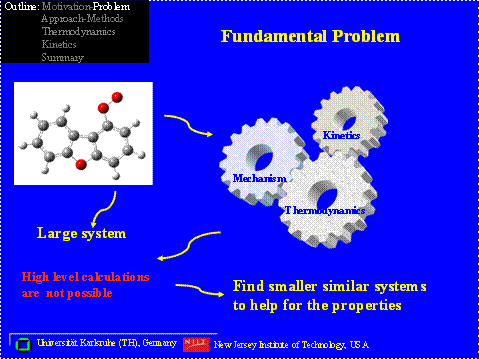
Ein Beispiel für die oxidative Zerstörung von Aromaten ist die Umwandlung von Dibenzofuranen und / oder Dioxinen in Verbrennungssystemen. Die Zerstörung des aromatischen Anteils beginnt oft mit dem Verlust eines Phenylwasserstoffs durch Abstraktion durch Radikalpoolspezies wie H, O, OH oder Cl, wobei ein Phenyl- oder Benzofuranylradikal gebildet wird. Dies geschieht selbst bei mäßigen Temperaturen in den nachgeschalteten Zonen eines Verbrennungsofens. Die Phenylradikale reagieren schnell mit molekularem Sauerstoff in der Verbrennungsumgebung und bilden ein energetisiertes (Phenylperoxy-)Addukt, das über mehrere Wege weiterreagieren kann. Abbildung 1 zeigt einige der Zwischenprodukte der Zersetzungsreaktionen (Beta-Spaltung (Unzipping) und Oxidation) eines formalen Benzofuran-Dialdehyd-Radikals, das als Hauptprodukt der Reaktion von molekularem Sauerstoff mit einem Dibenzofuran-Phenylradikal geschätzt wird. Die Zersetzungsreaktion führt zu einer Reihe von Zwischenprodukten und Radikalen, die keine thermochemischen Eigenschaften oder Gruppen haben, die für die Abschätzung der Gruppenadditivität verwendet werden können. Die Kenntnis der thermochemischen Eigenschaften dieser Spezies ist wichtig für das Verständnis der Zersetzungs- und Oxidationswege dieser Zwischenprodukte, die aus der anfänglichen oxidativen Ringöffnung der Aromaten resultieren.
Für solche größeren Moleküle sind Berechnungsmethoden auf hohem Niveau zu teuer oder nicht möglich. Die Dichtefunktionaltheorie ist möglicherweise eine der wenigen anwendbaren Berechnungsmethoden für diese großen Molekülsysteme.